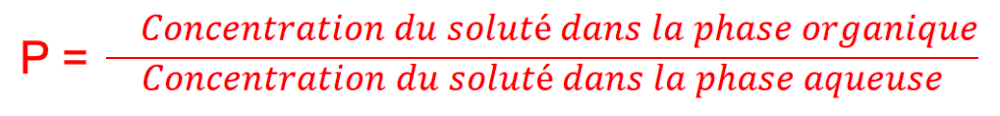✯La polarité mais aussi la présence de liaisons hydrogène dans la molécule influe la dissociation de celle-ci.
✯Lorsque la température de la solution augmente :
- si le soluté est solide, la solubilité augmente;
- si le soluté est gazeux, la solubilité diminue.
✯Lorsque la pression augmente, la solubilité augmente si le soluté est un gaz.
✯La solubilité d'un sel est diminuée si un ion de ce sel est déjà dans la solution : l’effet d'ion commun. loi de le chatelier
Exemple : dissolution de NaCl dans une solution où sont déjà introduits les ions Cl-
✯Le pH peut aussi influencer la solubilité: Le caractère acido-basique d’un composé moléculaire, ou des ions constitutifs d’un composé ionique peuvent directement influencer sa solubilité dans le solvant.
Permet de prédire le comportement d'un actif cosmétique dans une formulation :
Bioavailability : Un actif avec un coefficient de partage élevé peut être mieux absorbé par la peau.
Stabilité : Les ingrédients avec un bon équilibre de solubilité entre les phases hydrophile et hydrophobe peuvent contribuer à une formulation stable.
Exemple :
Vitamine E : Soluble dans les huiles (P élevé) et utilisée dans les formulations pour sa capacité à agir comme AO dans les phases lipidiques.
Acide Salicylique : Utilisé dans les formulations pour le traitement de l'acné, où son coefficient de partage permet une bonne pénétration à travers la peau tout en étant soluble dans des solvants aqueux.
▸ Un coefficient de partage de 0.01 indique que la vit C est 100 fois plus soluble dans l'eau que dans l'huile. Cela signifie qu'elle doit être formulée dans des bases aqueuses (comme des sérums ou des lotions) pour maximiser son efficacité.
✪ Stabilisation : repose sur plusieurs mécanismes
Interaction stériques : Des polymères ou des agents TA se placent autour des particules, empêchant leur agrégation.
Forces électrostatiques : Les particules chargées électriquement se repoussent, maintenant la dispersion.
✪ Déstabilisation :
Floculation : L'agglomération de particules en raison de forces d'attraction, souvent favorisée par des changements de pH ou de force ionique.
Coalescence : Fusion de gouttelettes dans une émulsion, pouvant entraîner la séparation des phases.