- Équilibrer les éléments autres que O et H.
- Équilibrer l’élément O en ajoutant des molécules d’eau H₂O du côté de la demi-équation où il manque de l’oxygène.
- Équilibrer l’élément H en ajoutant des ions H⁺ du côté de la demi-équation où il manque de l’hydrogène.
- Ajuster le nombre d’électrons pour assurer la conservation de la charge électrique.
Définition
Méthodologie
Méthode pour ajuster une demi-équation
Écrire et ajuster une équation redox entre 2 couples
- Écrire les demi-équations des deux couples.
- Ajuster les électrons.
- Combiner les demi-équations :
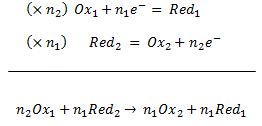
Il ne doit plus y avoir d'électrons qui apparaissent dans l'équation de la réaction d'oxyréduction !
A retenir :
L’oxydation est une perte d’électrons entraînant une augmentation du nombre d’oxydation, tandis que la réduction est un gain d’électrons avec une diminution du nombre d’oxydation. Un oxydant capte des électrons et se transforme en réducteur, alors qu’un réducteur donne des électrons et devient un oxydant. Les couples redox illustrent ces transformations, comme dans
.........................................................................................................................................................................................................
pour la réduction. Pour équilibrer une équation redox, il faut ajuster les éléments, les charges et les électrons.
