Bases azotées
= composés essentiels d'ADN et d'ARN, formée de bases puriques et pyrimidiques
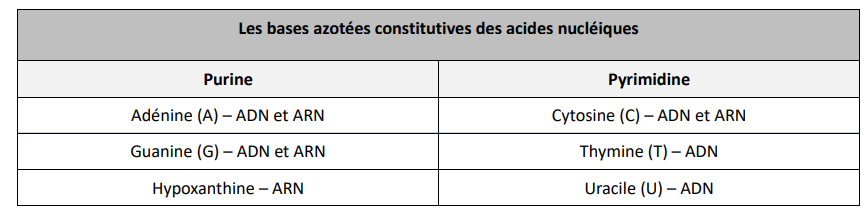
Bases puriques
- ADN et ARN : adénine, guanine
- autres : xanthine, hypoxanthine, acide urique = participent au catabolisme de l'adénine/guanine
Bases pyrimidiques
- ADN : cytosine, thymine
- ARN : cytosine, uracile
-> bases simples : bases puriques, pyrimidiques
-> bases combinées : nucléosides, nucléotides
-> autres bases mineures = caféine, théobromine
Rôle biologique
-constituants des acides nucléiques
-mise en réserve de l'énergie
-activation de précurseurs métaboliques dans les cascades enzymatiques
-médiateurs biologiques
-constutuants d'agents thérapeutiques anti-viraux
-> beaucoup de molécules sont analogues de ces bases = elles introduisent des erreurs dans la recopie du génome viral et donc ralentissent la prolifération virale
-> nombreuses anomalies métaboliques congénitales
= bases puriques causent les maladies
Bases combinés
-> nucléosides = bases azotées + ose liés par une liaison β-N-osidique
-> nucléotides : nucléosides phosphorylés (OH du ribose)
-> acides nucléiques : association de nucléotides (ADN et ARN)
- ADN = 2 brins complémentaires avec des liaisons H entre les bases - en double hélice
- ARN = simple brin mais qui peut s'associer avec un deuxième brin notamment dans les ARN viraux
Nucléosides, nucléotides, et acides nucléiques = caractéristiques métaboliques
-> purines et pyrimidines sont indispensables aux cellules
-> approvisionnement par un double mécanisme
- recyclage des bases libres
- = synthèse à partir de molécules partiellement détruites
- biosynthèse à partir de précurseurs
- = mécanismes différents entre purines et pyrimidines
-> apport alimentaire en purines et pyrimidines est facultatif mais nécessaire
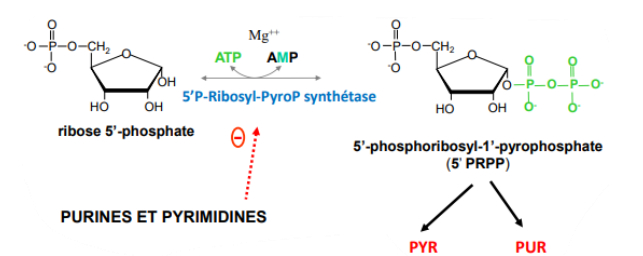
-> synthèse à partir du ribose-5-phosphate
- formation du PRPP
- sucre activé/ départ de la synthèse/ carrefour métabolique
- synthétisé à partir du ribose-P
- fait intervenir la PR-PP synthétase
-> catabolisme : différentes entre purines et pyrimidines
- purines dégradées en substances potentiellement toxiques
- élimination sous forme d'acide urique
- = sont toxiques
- pyrimidines dégradées en molécules facilement éliminées
-> ATP et GTP
- réservoir énergétique de la cellule
-> homéostasie
- équilibre de concentration de chaque nucléotides, formes désoxy
- = régulation enzymatique
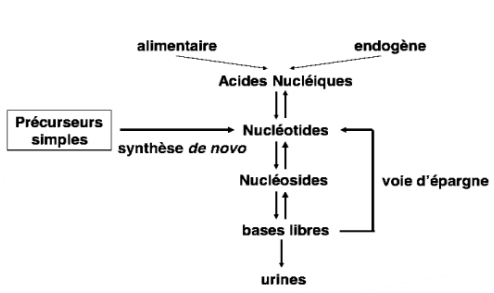
-> sources des bases ;
- exogène = alimentaire
- ADN digéré au niveau du tube digestif
- endogène
- auto-digestion de nos propres tissus
- à partir de précurseurs simples
Biosynthèse des nucléotides à purines
Biosynthèse selon la voie de novo = des purines
-> voie hépatique, cytosolique
- consomme de l'énergie
- production directe de nucléotides
- biosynthèse des ribonucléotides puis des désoxy ribonucléotides
-> mécanismes en 2 phases
- phase 1 : tronc commun
- part du α-D-ribose phosphate qui permet de synthétiser un amino-imidazole-ribonucléotide
- = produit final = acide inosinique
- phase 2 : transformation
- acide inosinique IMP utilisé pour subir diverses modifications afin de synthétiser de l'AMP ou de GMP
- AMP donnera ADP puis ATP
- GMP donnera GDP puis GTP
-> synthèse d'IMP
- se compose de 10 étapes
- à retenir : 1ère étape
- engage la biosynthèse
- = implication d'une PRPP glutamyl aminotransférase (PAT) - PAT prend en charge le PRPP + une glutamine et fixe un groupement NH2 sur ce PRPP libérant un pyrophosphate

=à partir d'un PRPP
-> de l'IMP à l'AMP
= on fait réagir l'IMP synthétisé avec de l'asparate et du GTP via une adénylosuccinate synthétase ce qui permet la synthèse d'un adénylosuccinate
-> pour la synthèse d'une AMP à partir d'un IMP, on consomme un ATP
-> de l'IMP au GMP
- IMP déshydrogénase intervient sur l'IMP permettant la synthèse d'un NADH, H+ = donne une xanthylate
- xanthylate interagit avec une glycine en présence d’ATP via une GMP synthétase pour donner un GMP
- quand on a une synthétase, on a forcément consommation d’énergie
-> pour la synthèse d’un GMP à partir d’un IMP, on consomme 1 ATP
Bilan de la synthèse de l'AMP ou de GMP à partir de l'IMP
= pour synthétiser un GMP ou AMP on consomme 7 ATP (on se place à partir de la synthèse d’IMP)
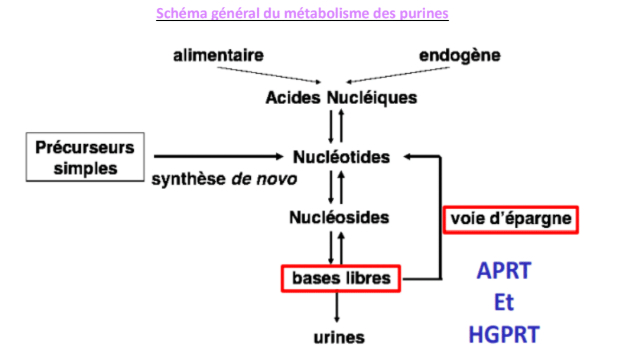
Biosynthèse selon la voie d'épargne ou de sauvetage
-> pour générer de l’AMP, on utilise l’adénine phospho ribosyl transférase (APRT)
-> pour générer du GMP, on utilise de l’hypoxanthine guanine phospho ribosyl transférase (HGPRT)
Récupération des nucléosides
= négligeable - ce ne sont pas les nucléosides que l'on récupère mais les bases azotées
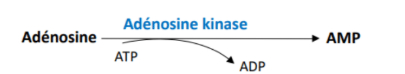
= va permettre de récupérer l'adénosine et la désoxy-adénosine grâce à une adénosine kinase (but est de récupérer l'adénosine et à partir d'un ATP de générer une AMP)
-> adénosine kinase dans les tissus périphériques assure la fonction très importante de resynthèse d'AMP à partir d'adénosine adressée par le foie
- foie synthétise l'adénosine et envoie dans la circulation sanguine - adénosine récupérée par les tissus et se serve de cette enzyme pour pouvoir former de l'AMP
Réactions de recyclage des bases puriques
= la + importante des 2 mécanismes de récupération - fait intervenir 2 enzymes clés afin de générer de l'AMP ou du GMP
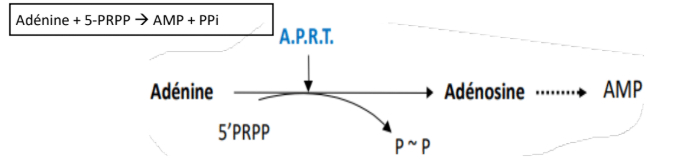
-> pour générer de l'AMP
- on utilise l'Adénine Phospho Ribosyl Transférase (APRT)
- APRT va prendre l'adénine et un 5'-PRPP pour donner AMP + PPi
-> pour générer du GMP
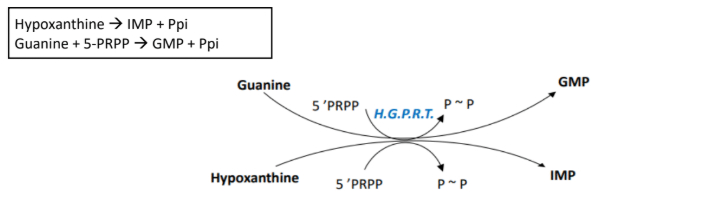
- on utilise l'Hypoxanthine Guanine Phospho Ribosyl Transférase (HGPRT)
- = permet de regénérer du GMP et de l'IMP
- HGPRT prend une guanine et un 5-PRPP pour donner un GMP + PPi
Conclusion
-> recyclage des bases puriques est intense dans les tissus à renouvellement rapide
- génère une importante économie d'énergie dans le sens ou la synthèse de novo d'AMP et de GMP consomme 7 ATP tandis que le recyclage ne consomme qu'1 ATP