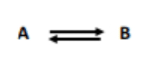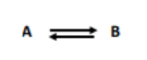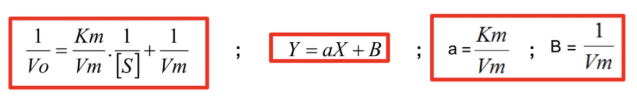Définitions
cinétique enzymatique = étude de la vitesse de la réaction et des paramètres susceptibles de la modifier
vitesse d'une réaction enzymatique =
- quantité de substrat (S) transformé par unité de temps
- ou
- quantité de produit (P) formé par unité de temps
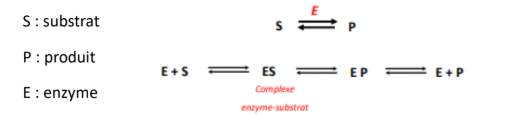
Déroulement d'une réaction enzymatique
-> produit est toujours lié à l'enzyme et n'est libéré qu'à la dernière étape
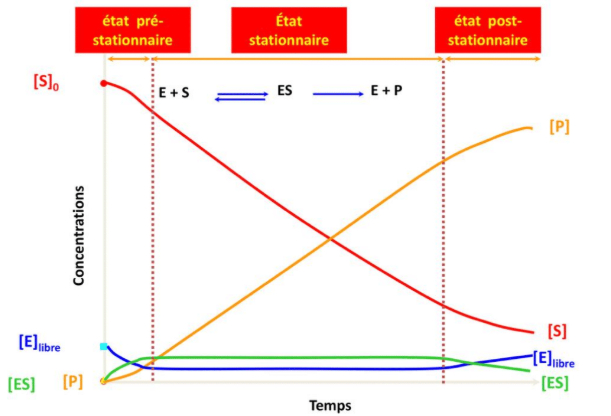
-> variation de [E], de [S] et de [ES] montrent que
- l'apparition du produit P reflète la disparition du substrat sur un plan quantitatif
- concentration de l'enzyme [E] diminue très vite à une valeur basse "constante" ([S] >> [E] Au moins un facteur 10)
- entre 2 instants t1 et t2, [ES] reste inchangée
- cette condition définit la phase stationnaire de la réaction
- la concentration totale d'enzyme [E]t = [E] + [ES]
Déroulement d'une réaction enzymatique (2)
-> phase pré stationnaire = phase de latence durant laquelle l'enzyme n'est pas encore chargée au max en substrat
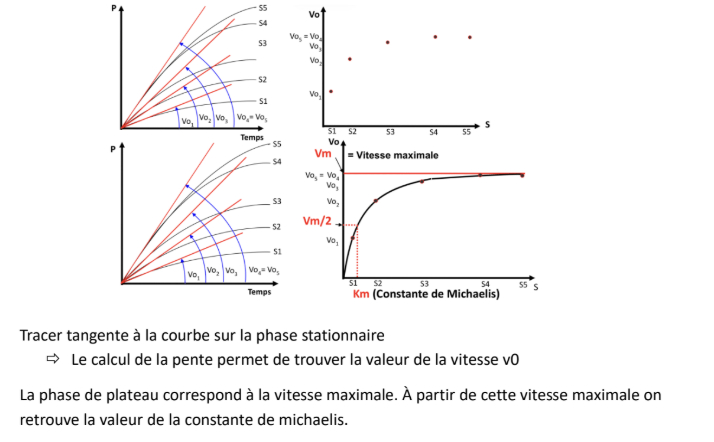
-> on s'intéresse à la phase stationnaire (linéaire) en mesurant la vitesse initiale
- max de molécules d'enzyme est lié avec le substrat
-> en phase stationnaire = une grande concentration d'enzyme chargée de substrat et une très faible concentration d'enzyme libre
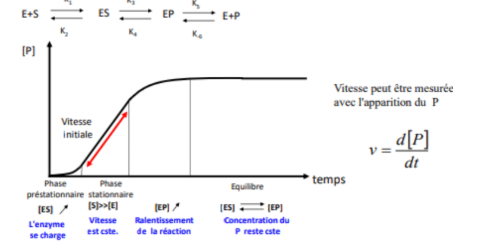
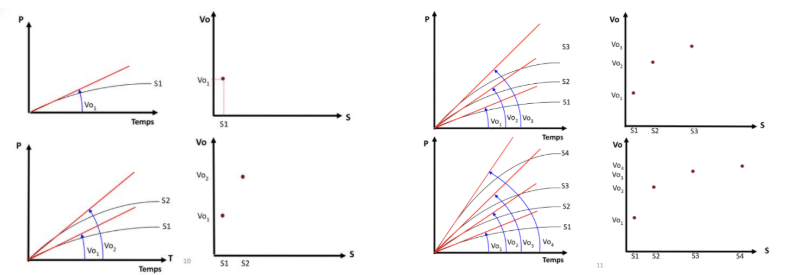
Détermination de la vitesse initiale (V0)
-> mesure d'absorbance du milieu réactionnel
-> temps de mesure
-> calcul de V0
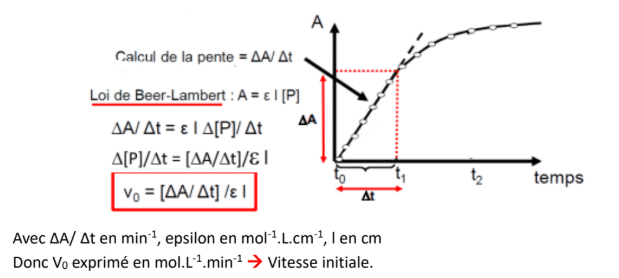
A : absorbance - t : temps - epsilon : coefficient d'absorption - P : produit - l : largeur de la cuve
Activité enzymatique ou catalytique
-> U = nombre de μmoles de substrat consommé par minute dans des conditions définies
nombre
-> kat : nombre de moles de substrat consommé par seconde dans des conditions définies
- 1 kat = 1 mol.s-1
- 1 U = 1 μmol. min-1 = 16,67 nmol.s-1 ou 1 nkat = 60.10-3 U
Concentration d'activité enzymatique ou catalytique (Ccat)
-> Ccat = μmoles ou moles de substrat transformé par min ou sec respectivement par unité de volume de solution enzymatique
-> concentration d'activité enzymatique est plus souvent utilisée pour l'analyse de prélèvements de biologique médicale par ex
= correspond finalement à une vitesse initiale
Constante catalytique (Kcat)
= traduit le nombre de moles de substrat transformées par mole d'enzyme et par seconde
Activité spécifique (AS)
= quantité de substrat transformée par unité de temps et par masse d'enzyme
- peut-être exprimée en U.mg-1 d'enzyme
Activité molaire spécifique (AMS)
= quantité de substrat transformé par unité de temps et par mole d'enzyme
Vitesse maximale Vm de la réaction et constante d'affinité de l'enzyme pour le substrat Km
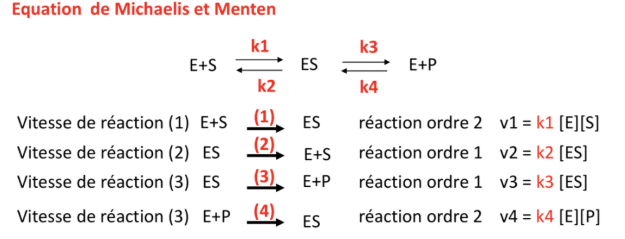
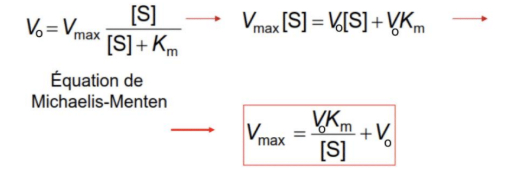
Equation de Micahelis et Menten
Notion d'ordre des réactions (vitesse "v")
-> réaction d'ordre 0
- transformation d'un seul substrat en un produit
- v = constante au cours de la diminution de la concentration du substrat [A]
-> réaction d'ordre 1
- transformation d'un seul substrat en un produit
- v est directement proportionnelle à la concentration du substrat [A]
- v = k[A]
- k = constante de vitesse
-> réaction d'ordre 2
- deux substrats qui réagissent l'un avec l'autre pour donner un produit
- v est proportionnelle au produit des concentrations des substrats [A] et [B]
- v = k [A] [B]
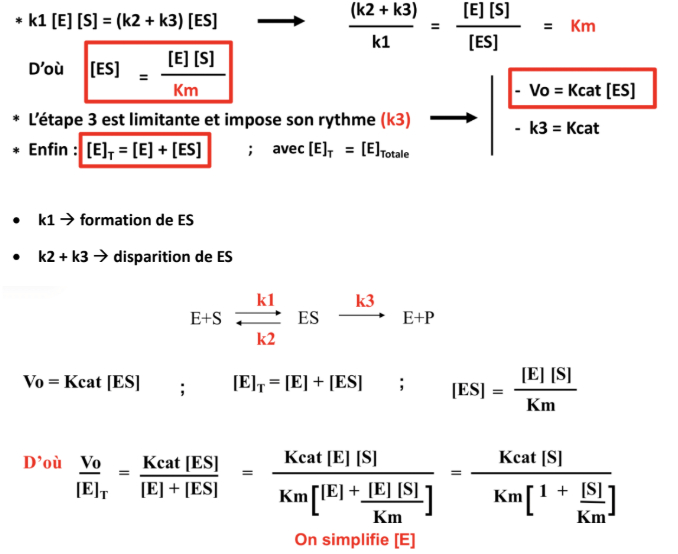
-> on néglige l'étape 4 = k4 [E] [P] dans les conditions initiales
- [P] est négligeable car pas assez de produit pour formé que l'étape se fasse dans l'autre sens puisque l'on est en phase stationnaire
-> [ES] constante = plus qu'une réaction qui peut donner ES
-> à l'équilibre, vitesse de transformation ES = vitesse de disparition de ES
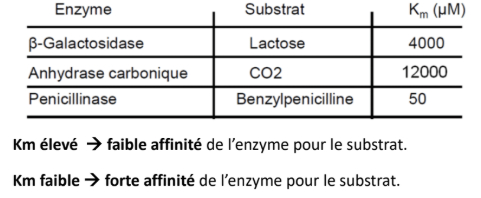
-> constante de Michaelis Km
= caractéristique d'un couple enzyme-substrat et dépend des conditions expérimentales
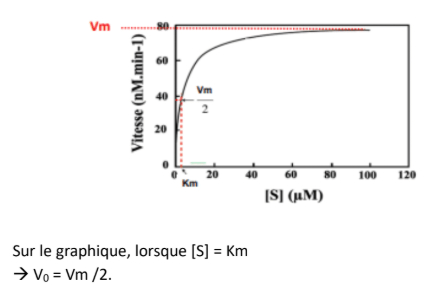
Signification de Km et Vm
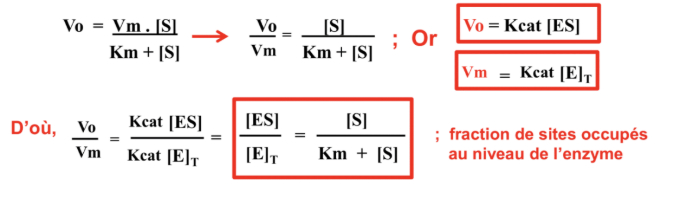
-> application de la relation de Michaelis
- V0 = Vm.[S] / Km + [S]
- quand [S] = km - V0 = Vm.Km / Km+Km
- -> V0 = Vm/2
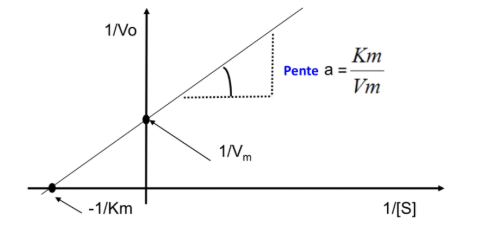
Représentation de Lineweaver-Burk
-> permet de tracer un graphique 1/V vs 1/[S] dont la courbe = une droite (y = ax + b) pour les enzymes obéissant à la relation Michealienne entre vitesse de réaction et concentration du substrat
-> la droite coupe l'axe des x en -1/Km
-> la droite coupe des y en 1/Vm
-> la pente de la droite est Km/Vm
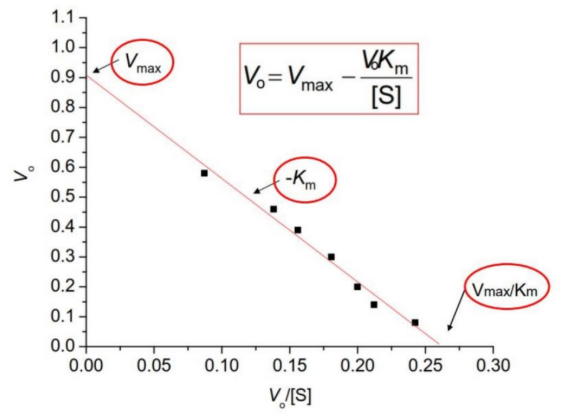
-> linéarisation d'Eadie-Hofstee
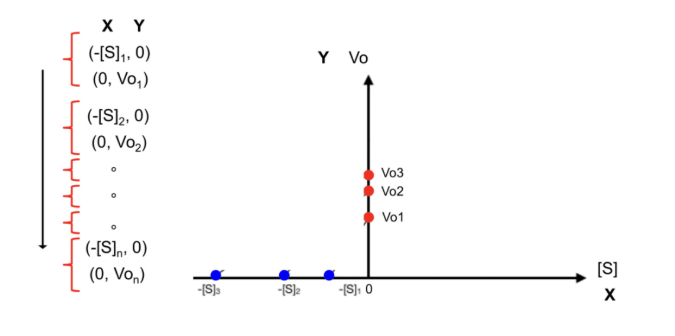
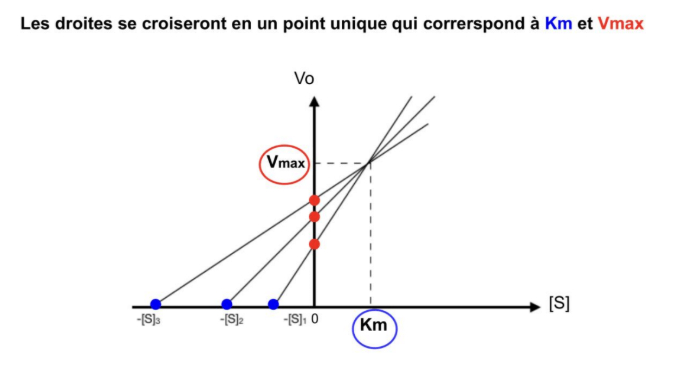
-> représentation selon Eisenthal et Cornish-Bowden
ici chaque paire de coordonnées donne des valeurs uniques d'abscisse à l'origine et d'ordonnée à l'origine et de pente