Définition
Atome
La plus petite unité de la matière qui conserve l'identité d'un élément chimique.
Noyau
La partie centrale d'un atome, constitué de protons et de neutrons.
Proton
Une particule subatomique portant une charge positive, située dans le noyau de l'atome.
Neutron
Une particule subatomique neutre, située dans le noyau de l'atome.
Électron
Une particule subatomique portant une charge négative, orbitant autour du noyau.
Ion
Un ion est un atome ou une molécule qui a gagné ou perdu un ou plusieurs électrons, ce qui lui confère une charge électrique nette positive ou négative. Les ions positifs, appelés cations, ont perdu des électrons, tandis que les ions négatifs, appelés anions, en ont gagné. Les ions jouent un rôle crucial dans divers processus chimiques et biologiques, notamment dans la conduction électrique, les réactions chimiques et le maintien de l'équilibre électro
Structure de l’Atome
Chaque atome est constitué d'un noyau contenant des protons et des neutrons, entouré d'électrons en orbite. Les protons possèdent une charge positive tandis que les neutrons sont neutres, ce qui confère au noyau une charge globale positive. Les électrons, portant une charge négative, gravitent autour du noyau et leur disposition détermine la manière dont l'atome interagit avec d'autres atomes.
Propriétés des Ions
Lorsqu'un atome gagne ou perd des électrons, il devient un ion. Un atome qui perd un ou plusieurs électrons devient un cation, dotée d'une charge positive. Inversement, un atome qui gagne des électrons devient un anion, avec une charge négative. Ces changements de charge influencent grandement les propriétés chimiques de l'atome, en particulier sa réactivité et sa capacité à se lier avec d'autres atomes.
Formation des Ions
Les ions se forment souvent par des interactions chimiques où des électrons sont transférés entre atomes. Ce transfert est couramment observé dans les liaisons ioniques, où un atome perd un électron pour devenir un cation et un autre atome gagne cet électron pour devenir un anion, comme dans le chlorure de sodium. La tendance d'un atome à former des ions est influencée par sa structure électronique et son énergie d'ionisation.
L'Interaction entre Atomes et Ions
Les interactions entre les atomes et les ions sont essentielles à la formation de composés chimiques. Par exemple, les liaisons ioniques résultent de l'attraction électrostatique entre des cations et des anions. Cette interaction est fondamentale dans la chimie des sels et influence de nombreuses propriétés physiques comme le point de fusion et la solubilité.
Applications et Importances des Ions
Les ions jouent un rôle crucial dans divers processus biologiques et industriels. Dans les organismes vivants, ils sont essentiels pour le transport de l'influx nerveux, la contraction musculaire et l'équilibre osmotique. Industriellement, ils sont utilisés dans des batteries, le traitement de l'eau et de nombreuses réactions de synthèse chimique. Ainsi, la compréhension des ions et de leur comportement est fondamentale dans de nombreux domaines scientifiques et technologiques.
A retenir :
Les atomes sont les unités de base de la matière, formés d'un noyau central entouré d'électrons. Lorsqu'ils gagnent ou perdent des électrons, ils deviennent des ions, chargés positivement ou négativement. La formation et l'interaction des ions sont à la base de nombreux phénomènes chimiques, avec des applications vitales dans la biologie, la chimie industrielle et la technologie.
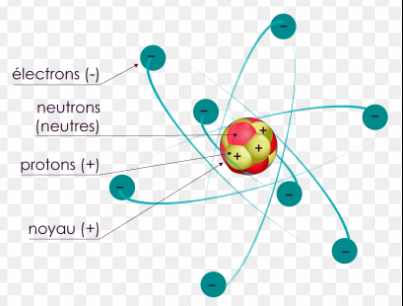
les principaux composants d'un atome

