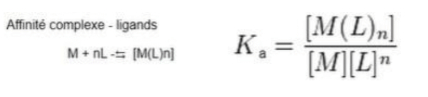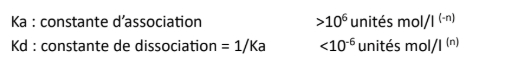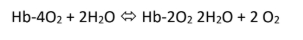Nomenclature
-> nombre de ligands : di, tri, tétra, penta, hexa
-> ligands anioniques = se terminent toujours par "o"
- Cl- : chloro-
- OH- : hydroxo-
- S2O2- : thiosulfato
-> ligands neutres -> peu modifiés
- H2O : aqua
- NH3 : ammine
- NO : nitrosyle
-> nom du métal :
- 2 possibilités
- ensemble du complexe neutre ou positif = pas de variation du nom
- complexe négati
-> charge initiale de l'ion métallique en chiffre romain

exemple
Ligand polydentiques = ligands chelateurs
-> le ligand peut mettre en place plusieurs positions de coordination à l'ion métallique
= aussi appelé ligands chélateurs
Ion oxalate (Ox)2-
-> acide oxalique HOOC-COOH, diacide classique mais lorsque ce diacide est déprotoné = capable de mettre en place 2 liaisons de coordination
Ethylène diamine
-> NH2-CH2-CH2-NH2
-> éthylène diamine :
- cobalt au centre
- 6 liaisons de coordination
- trans car 2 atomes de chlore opposés
- = on en déduit que le cobalt est 3x positif
EDTA4-
-> antidote : empoisonnement à Pb, Hg
-> conservateur : alimentaire, collyres
-> réactif analytique
-> détergents et lessives
-> décontamination de radioactivité
Stabilité
-> on définit l'affinité entre le complexe et les ligands
- pour casser une liaison covalente en chimie analytique on augmente les T°C
-> 2 constantes équivalentes
-> constante d'association est souvent très élevé
- à l'inverse les constantes de dissociations sont très faibles = inf à 1
-> pour les valeurs plus simples de Kd on utilise : pKd = -log (Kd)
- plus le pKd est grand - plus le Kd est petit et plus complexe est satble
- = + stable + sont activité sera importante
Propriétés biologiques
Transport de ligands
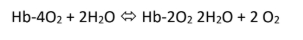
-> hémoglobine peut transporter 4 dioxygènes pour former l'oxyhémoglobine mais en présence d'eau et de moins de dioxygène = 2 molécules d'O2 seront remplacées par 2 molécules d'H2O pour former la désoxyhémoglobine
-> lorsqu'un métal toxique dans l'organisme = on ajoute un médicament qui va complexer le métal pour favoriser son élimination et réduire sa toxicité
- certains métaux peuvent changer de ligand comme l'Hg, Hg2+ et CH3-Hg+ qui vont former des complexes avec des thiols en fonction de l'affinité
- ces ligands sont appelés des mercaptans
-> Valinomycine (ATB) = inosphère à K+
- provoque un trou dans la membrane spécifique du potassium - fuite de potassium
Intérêt catalytique
-> metalloprotéine = catalyseurs enzymatiques
- diminue l'énergie d'activation -> + vitesse d'augmentation d'un substrat + sélectité
- permet de catalyser la réaction enzymatique
Substance actives pharmaceutiques
-> cisplatine, carboplatine : liaisons de coordination avec double hélice - bloquent la mitose = antimitotique
-> complexation d'agents toxiques : capture et élimination = sont des antidotes capables de capter les métaux lourds permettant ainsi leur élimination
Agents de contraste en IRM : gadolinium Gd+++
-> rappel : 3 grandes méthodes d'imagerie
- scanner = simple radio - différencie les os des tissus mous car voit le Ca des tissus osseux
- principe du contraste qui permet de différencier les tissus qui nous intéresse de ce qui nous intéresse pas
- scintigraphie par émissions de positions = détecte et fait une reconstitution spatiale du tissu ou de l'organe
- scintigraphie par émissions de rayonnements bêta = administration d'un élément radio qui émet des e-, caméra qui les photographie et reconstitue la géométrie de l'organe
- IRM : utilisation d'un champ magnétique et mesure les atomes qui vont être perturbés par ce champ
-> Gd3+ complexe H2O
- accélère leurs temps de relaxation T1 et T2 des H
- améliore le contraste des images en IRM
-> Gd3+ en compétition avec Ca++
- activité cardiaque, musculaire, coagulation sanguine = très toxique
-> pb : très toxique - entre en compétition avec le Ca ce qui va perturber l'activité cardiaque et musculaire et la coagulation sanguine
- on le complète pour diminuer sa toxicité
- = encaspulation très forte pour qu'il ne se libère pas dans l'organisme
-> utilisation : rupture de la BHE - diagnostic des tumeurs cérébrales, tumeurs de la moelle, osseuse, hépatique
Ions dans les milieux biologiques
-> métaux toxiques dans l'organisme
- médicaments vont être des agents de complexation ou chélateurs ce qui favorise son élimination et réduire sa toxicité
- but est d'éliminer le métal, on estime que le métal chélaté est + facile à éliminer par voie rénale
Environnement des ions
-> Na+ et K+ sont hydratés dans l'organisme = être entourés de molécules d'eau mais sans liaisons = interactions électrostatiques peu stables donc pas de complexes libres dans le plasma sauf dans le cas de la valinomycine
-> Ca2+ et Mg2+ sous 2 formes :
- soit hydraté
- soit complexés
-> autres = complexes avec molécules endogènes
- tel que l'albumine qui est une molécule sanguine retrouvée dans le plasma
Différentes affinités
-> lorsqu'un métal toxique présent dans notre organisme = on ajoute un médicament qui va complexer ce métal pour favoriser son élimination et réduire sa toxicité
- lorsqu'on a un ion métallique associé à une molécule endogène = on ajoute un ligand avec une affinité supérieur qui va entraîner un déplacement de l'association de l'ion vers le ligand
-> déféroxamine chélate le Fe dans :
- l'hémosidérine
- ferritine
- transferine
-> mercaptans (vient de Mercury capture) = petites molécules soufrées à groupement thiol (-SH) qui capturent le complexe
Ionisation et solubilité
-> lorsqu'on a un métal et qu'on ajoute un ligand :
- ligand neutre = ne modifie pas la charge
- ligand chargé = neutralise une charge +
- on peut neutraliser la charge + du métal si on a un ligand chargé -
-> ex :
- calcium chargé 2 fois positivement = soluble
- -> on veut l'administrer par VO mais n'est pas assimilé facilement par le système digestif = on va l'associer au gluconate (acide faible) pour lui faire perdre ses charges + car par VO, idéal est d'avoir un complexe/une molécule soluble et non-chargé/neutre
- = va pouvoir complexer au Ca
- on a 2 gluconates pour 1 Ca cela fait une annulation des charges
- sans charges = c'est plus assimilable par le système digestif
- gluconate :
- idée est d'apporter du Ca non chargé sous forme de glutonate
- même principe avec le zinc car chargé 2 fois +
- complexes charges permettent un meilleure assimilation par voie orale
Ligand de type dur, sans souffre
Chélateur de plomb
= le + utilisé et un dérive de l'EDTA
-> on l'associe au Ca et au Na pour équilibré la charge
-> complexe avec le Ca va chélater le plomb et d'autres métaux lourds pour être utiliser comme principal médicament comme le saturnisme
-> affinité de l'EDTA pour le plomb va être sup à celle du Ca donc Ca sera libéré et le plomb sera chélaté
-> médicament est administré par perfusion IV
- Pb-EDTA et Zn-EDTA sont éliminés par les urines et un apport en zinc compensatoire afin d'éviter toute carence se fera à la suite du ttt par voie orale
Chélateur de cyanure
-> possibilité d'avoir une intoxication au cyanure = toxique car toute petite molécule qui diffuse facilement
- + elle est petite + elle diffuse facilement
-> toxicité immédiate
- cyanures complexent le Fe3+ à l'aide de la cytochrome oxydase mitochondriale = bloque la respiration cellulaire = arrêt cardiaque voir mort
-> pour s'en débarrasser = on peut administrer du cobalt par IV
- cobalt possède une forte affinité pour le cyanure = capable de le chélater
- utiliser sous forme d'hydroxocobalamine - vit B12
-> ttt par voie injectable pour avoir un effet le plus immédiat possible
Chélateur de fer
= on essaye de le chélater dans le cas de différentes pathologies où nous avons une saturation en fer dans le plasma
- hémolyse = hémoglobine libère le fer dans le sang
- déféroxamine - DESFERAL
- ne contient pas de fer mais capture/complexe le fer et devient la feroxamine qui est ensuite éliminée dans les urines
- utilisé dans le ttt de première intention lors d'une surcharge plasmatique ou cellulciare
- 3 indications :
- thalassémie majeure
- hémochromatose
- intoxication en aluminium
-> fer plasmatique : excrétion urinaire de la feroxamine
-> fer hépatique : élimination fécale
Sidérophore
-> chélateur principal
-> produit par Streptomyces pilosus
-> 3 fonctions acide hydroxyamique qui permettent de capturer le fer en repliant sur elle même
Autres complexes qui permette de capturer le fer
-> déférasirox - EXJADE
- chélateur tridenté du Fe3+
- 2 ligands pour 1 ions Fe3+
- administré par VO
- éliminé par voie biliaire : permet de diminuer la quantité de fer tissulaire hépatique
- chélate aussi l'aluminium
- utilisé lors de transfusions sanguines fréquentes qui entraînent des surcharges en fer
-> défériprone I - FERRIPROXE
- chélateur bidenté
- 3 ligands pour 1 fer
- administration par VP
- ttt de la thélassémie
- activité dans la maladie de Parkinson où il pourra chélater le fer excédentaire au niveau encéphalique
Chélateurs soufrés R-SH
-> auront une grande affinité pour : As, Hg, Cd, Bi
-> mercapto = molécule qui capture le mercure
-> dimercaprol - B.A.L
- antagoniste des gaz à base d'arsenic
- administré par voie IM
- chélateur de métaux lourds grâce aux fonctions thiol
- utilisé comme antidote contre les intoxications à l'arsenic, mercure, étain, plomb
- 2 groupements SH
-> D.penicillamine - TROVOLOL
- chélate le Cu, Zn, Hg, Pb pour augmenter leur excrétion urinaire
- un groupement SH
- thioréducteur = rompt les ponts disulfures des macroglobulines
- entraîne une dépolymérisation des facteurs rhumatoïdes IgM
- modifie leur activité biologique
- administré par VO
- indications :
- anti-rhumatismal dans les polyarthrites rhumatoïdes
- immunosuppresseur
- maladie de Wilson : accumulation de Cu
- chélate le cuivre pour faciliter l'élimination urinaire
-> succiner (acide dimercaptosuccinique ou DMSA) - SUCCICAPTAL
- chélateurs des intoxications au Hg, Pb, As
- possède 3 isomères qui n'en forment finalement que 2
- utilisé ++ pour les intoxications au mercure
- obtenu par addition de groupements SH sur l'acide succinique
- administration par VO
- élimination urinaire des métaux lourds
- point positif : n'augmente pas le passage du plomb dans l'encéphale
Médicaments : chélateurs échangeurs d'ions
-> polystyrène sulfonate de sodium PPS - KAYEXALATE
- administré lors d'hyperkaliémies
- par VO ou VR
- capture le potassium
- dans l'intestin :
- libère Na+
- fixe K+
- élimination dans les matières fécales
- poso : 15g adaptée selon la kaliémie
-> sevelamer - RENAGEL
- chélate le phosphate dans le domaine gastro/intestinal
- réduit la concentration de phosphate plasmatique
- utilisé lors d'une hyperphosphatémie
= résine, polymère solide qui à la particularité de capturer des ions phosphates puis éliminer
-> colestyramine - QUESTRAN
- résine chélatrice des sels biliaires comme acide cholique
- administré lors d'hypercholestérolémie
- complexe les acides biliaires intestinaux
- organisme synthétise de nouveaux acides biliaires et puis dans les réserves de cholestérol
- effet hypocholestérolémiant
- = collecte des sels biliaires
-> acides biliaires :
- émulsionnent les lipides
- proviennent du cholestérol endogène
-> lorsque l'organisme à besoin de produire des sels biliaires il puise à partir des réserves de cholestérol de l'organisme d'où sont effet hypo