L’enthalpie libre ou la fonction de Gibbs est une fonction d’état qui a une grande importance en chimie car elle permet de prédire si une réaction est thermodynamiquement possible ou non. Elle est notée G.
Lorsque le système évolue spontanément la valeur de la fonction enthalpie libre qui le caractérise diminue jusqu’à une valeur minimale et on peut assimiler cette fonction à un potentiel :
si ΔG < 0, le système évolue spontanément
si ΔG > 0, le système ne peut évoluer spontanément
si ΔG = 0, le système est en équilibre.
Les réactions thermodynamiquement spontanées sont des réactions exergoniques (ΔrG < 0). Celles qui ne le sont pas sont des réactions endergoniques (ΔrG > 0).
Une réaction spontanée est une réaction thermodynamiquement possible avec un
ΔrG < 0. Elle évolue sans apport d’énergie extérieure sous forme de travail. Attention : cela ne veut pas dire que la réaction soit nécessairement très rapide.
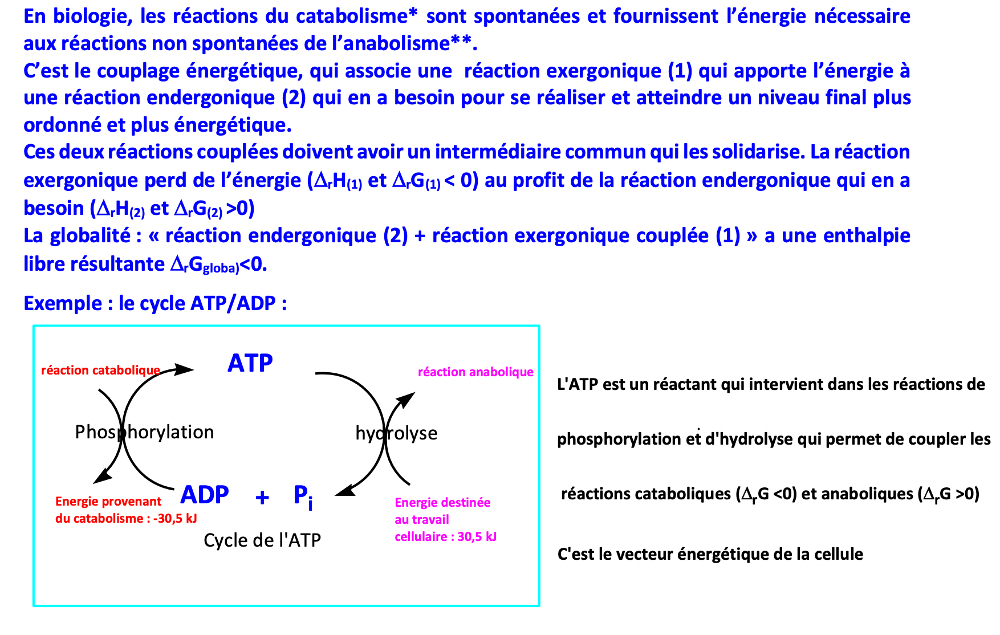
Pour réaliser une réaction qui n’est pas spontanée (ΔrG > 0), il est possible de la coupler avec une réaction exergonique (ΔrG < 0).
Une réaction est quasi-totale ou quantitative lorsque sa constante d’équilibre K >> 1. Concrètement si l’on part d’un nombre de mole (ou d’une concentration égale) de chaque réactif, elle est quasi- totale ou quantitative s’il reste à la fin de la réaction 1% ou moins de 1% de la quantité de matière des réactifs initiaux. La constante K pour une réaction où les coefficients stœchiométriques sont tous égaux à 1 (cas des équilibres acido-basiques) sera ≥ 10 puissance 4.
Remarque : Pour les réactions d’oxydo-réduction pour lesquelles les coefficients stœchiométriques peuvent être différents de 1 et non égaux, ce critère n’est plus valable et il faut à chaque fois calculer K selon la stœchiométrie pour avoir 1 ?% ou moins de 1% des réactifs initiaux.