La notation de Lewis d’un atome est un modèle qui représente son symbole
chimique ainsi que ses électrons de valence.
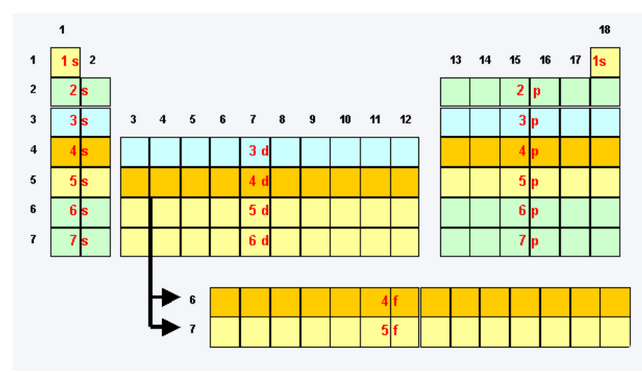
- Le remplissage des couches se fait dans l'ordre d'énergie croissant, c’est-à-
dire s, puis p, puis d et enfin f
- Une couche ne commence à se remplir que si la couche précédente est
saturée (règle de stabilité)
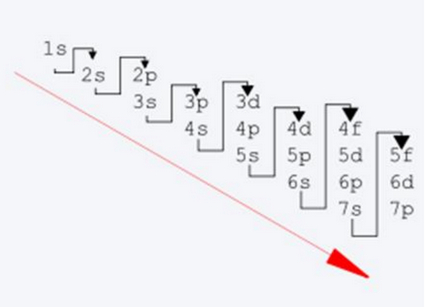
Remplissage des couches électroniques
-Les électrons de valence correspondent aux électrons qui appartiennent
à la dernière couche.
-Les autres électrons sont dits de cœur.

Rouge: électrons de valence Vert: électrons de coeur
La notation de Lewis d’un atome est un modèle qui représente son symbole
chimique ainsi que ses électrons de valence.
Les électrons de valence sont symbolisés par des points autour du symbole de
l’atome.
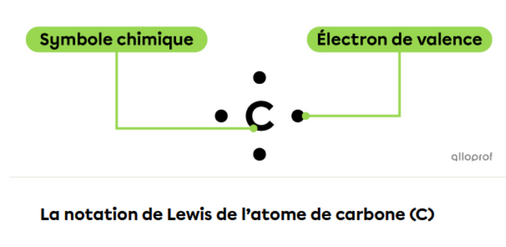
• Lorsqu’il existe une différence d’électronégativité entre 2 atomes liés
par une liaison covalente, les 2 électrons impliqués dans cette liaison
ne se répartissent pas symétriquement entre les 2 atomes mais ont
tendance à se rapprocher de l’atome le plus électronégatif.
• Cette dysmétrie entraîne la création de charges partielles delta – (du
côté de l’atome le plus électronégatif) et delta + (de l’autre).

- Le remplissage des couches se fait dans l'ordre d'énergie croissant, c’est-à-
dire s, puis p, puis d et enfin f
- Une couche ne commence à se remplir que si la couche précédente est
saturée (règle de stabilité)

Remplissage des couches électroniques
-Les électrons de valence correspondent aux électrons qui appartiennent
à la dernière couche.
-Les autres électrons sont dits de cœur.

Rouge: électrons de valence Vert: électrons de coeur
La notation de Lewis d’un atome est un modèle qui représente son symbole
chimique ainsi que ses électrons de valence.
Les électrons de valence sont symbolisés par des points autour du symbole de
l’atome.


• Lorsqu’il existe une différence d’électronégativité entre 2 atomes liés
par une liaison covalente, les 2 électrons impliqués dans cette liaison
ne se répartissent pas symétriquement entre les 2 atomes mais ont
tendance à se rapprocher de l’atome le plus électronégatif.
• Cette dysmétrie entraîne la création de charges partielles delta – (du
côté de l’atome le plus électronégatif) et delta + (de l’autre).
