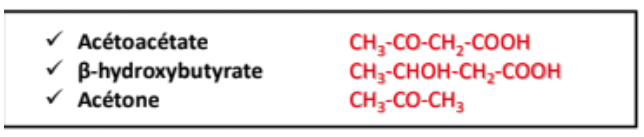
-> 3 corps cétoniques métabolisables
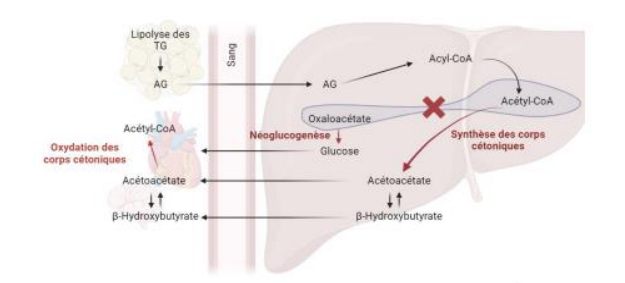
-> métabolisme des corps cétonique =
- synthèse à partir d'acétyl-CoA = cétogenèse provenant de la β-oxydation des AG
- catabolisme en acétyle-CoA = cétolyse qui nécessite une entrée dans le cycle de Krebs
-> quand pénurie de glucose = néoglucogénèse est enclenchée mais le glucose produit est réservé aux tissus glucodépendants
- plupart des organes consomment des AG
-> cétogenèse exclusivement dans le foie
-> cétolyse a lieu dans le myocarde, muscles, foie, cerveau, cortex rénal
-> cétogenèse est faible en temps normal
- situations métabolique physiologique = jeûne, malnutrition
- ou pathologiques = diabète sucré non équilibré
- = activée = conditions de cétoses
-> conditions normales : production des CC est faible mais peut devenir pathologique dans le cas où l'organisme ne peux plus s'en débarrasser
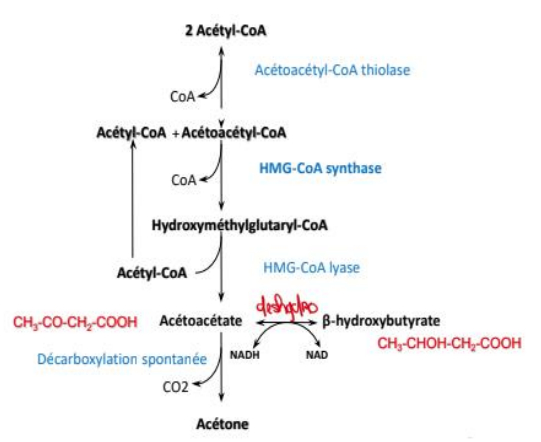
Synthèse des corps cétoniques
Origine de l'acétyl-CoA
-> peut provenir des graisses
- quand lipolyse adipeuse importante, AG libres arrivent ou foie ou subissent la β-oxydation = acétyl-CoA
-> peut provenir des AA = 3 groupes d'AA cétoformateurs
- qui conduisent à l'acétoacétate : Tyr, Leu, Phe
- ceux qui conduisent à l'acétoacyl-CoA : Lys, Trp
- ceux qui donnent un pyruvate et/ou acétyl-CoA : Ala, Gly, Ser
= 1er corps formé = Acétoacétate
Catabolisme des corps cétoniques
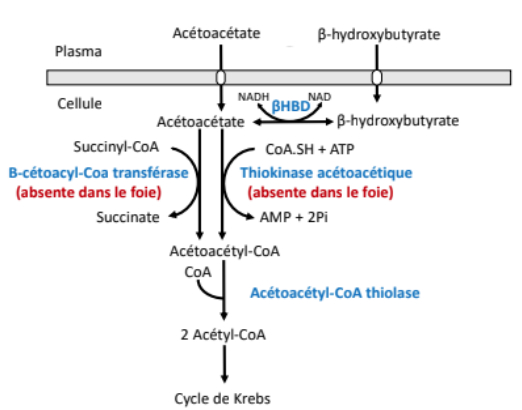
-> CC peuvent diffuser à travers la membrane = pas besoin de récepteurs
-> CC synthétisés dans le foie = il ne faut pas que le foie les consommes juste après
- = foie dénué de la β-cétoacyl-CoA transférase et de la thiokinase acétoacétique
- incapable de cataboliser les CC = les déverse dans la CG
-> catabolisé par coeur, reins, cerveau, muscles
Régulation de la cétogenèse
Acétyl-CoA
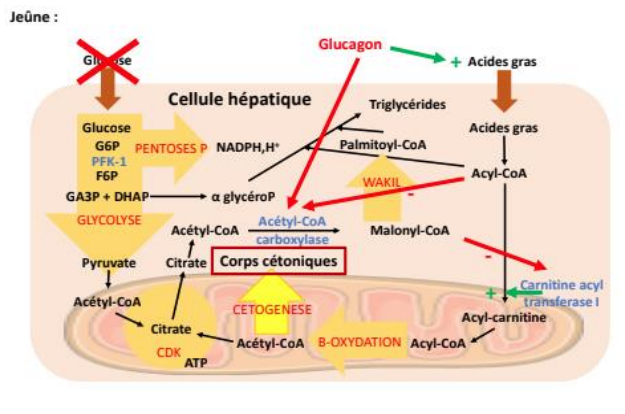
-> lipolyse activée dans le tissu adipeux suite à la modification du rapport insuline/glucagon -> libération d'AG
-> AG capté par :
- tissus consommateurs
- foie = cétogenèse
-> acyl-CoA inhibe l'acétyl-CoA carboxylase
- diminue la concentration en malnolyèCoA
- lève l'inhibition qu'exerce celui-ci sur la carnitine acyl transférase
- acyl-CoA entrent dans la mitochondrie et subissent la β-oxydation
- production d'acétyl-CoA qui pourront entrer dans la cétogenèse
Oxaloacétate
-> apport glucidique insuffisant :
- taux issu du pyruvate provenant de la glycolyse baisse
- = freine l'entrée de l'acétyl-CoA dans le CDK
- oxaloacétate provenant du pyruvate de la néoglucogénèse est entièrement dédié à celle-ci
- = pas d'utilisation possible de l'acétyl-CoA dans le CDK par manque d'oxaloacétate
= acétyl-CoA s'engouffre dans la cétogénèse
Cétogenèse pathologique
Cas des diabètes
-> tissu adipeux
- = déséquilibre entre insuline et hormones hyperglycémiantes
-> activation de la triglycéride lipase et production d'AG à partir des TG
-> passage des AG dans le sang
Foie
-> sérum albumine amène une grande quantité d'AG
- foie incapable de réinsérer dans les TG
- β-oxydation accélérée
- acétyl-CoA produit ne pourra pas servir à la re-synthèse d'AG par déficit en NADP réduit
= reconstitution des stocks de glycogène et maintien de la glycémie à un niveau normal avec augmentation de néoglucogénèse au niveau des AA
Tissus périphériques
-> arrivée massive du CC en provenance du foie
- saturation du catabolisme au niveau des muscles, coeur
- la β-cétoacyl-CoA transférase a besoin du succinyl-CoA or CDK est déficitaire
- catabolisme des CC va donc être réduit
- = élimination rénale
-> au niveau de tous les tissus
- augmentation de la protéolyse pour former du glucose à partir des AA glucoformateurs
- libération simultatnée d'AA cétoformateurs = production de CC
Traitement de la cétose
-> cas du jéûne
= manger du sucre ou saccharose
-> cas du diabète
= pour le DT1 -> il faut restaurer une insulinémie normale
- en cas d'acidose on donne un ttt alcalinisant par perf de soluté bicarbonaté ou de tham
-> attention : insuline agit très mal en cas d'acidose = il faut d'abord remonter le pH
Autres causes de la cétose
-> glycogénolyse de type I
- déficit en glucose-6-phosphate
-> leucinose
- déficit de l'enzyme céto-acide-décarboxylase
